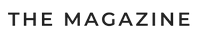Kenaikan harga sumber tenaga merangsang pencarian jenis bahan bakar yang lebih cekap dan lebih murah, termasuk di peringkat isi rumah. Kebanyakan pengrajin yang berminat tertarik dengan hidrogen, yang nilai kalori tiga kali lebih tinggi daripada metana (38,8 kW berbanding 13,8 dengan 1 kg bahan). Kaedah pengekstrakan di rumah, nampaknya, sudah diketahui - pemisahan air dengan elektrolisis. Sebenarnya, masalahnya jauh lebih rumit. Artikel kami mempunyai 2 tujuan:
- untuk menganalisis persoalan bagaimana membuat penjana hidrogen dengan kos minimum;
- pertimbangkan untuk menggunakan penjana hidrogen untuk memanaskan rumah persendirian, mengisi minyak kereta, dan sebagai mesin kimpalan.
Bahagian teori ringkas
Hidrogen, aka hidrogen, - unsur pertama jadual berkala - adalah bahan gas yang paling ringan dengan aktiviti kimia yang tinggi. Semasa pengoksidaan (iaitu pembakaran) ia mengeluarkan sejumlah besar haba, membentuk air biasa. Kami mencirikan sifat elemen, merancangnya dalam bentuk tesis:
- Pembakaran hidrogen adalah proses yang mesra alam, tidak ada bahan berbahaya yang dilepaskan.

- Oleh kerana aktiviti kimianya, gas bebas tidak berlaku di Bumi. Tetapi dalam komposisi air rizabnya tidak habis-habisnya.
- Unsur tersebut diekstrak dalam pengeluaran industri dengan kaedah kimia, misalnya, dalam proses gasifikasi (pirolisis) arang batu. Selalunya produk sampingan.
- Kaedah lain untuk mendapatkan hidrogen gas adalah elektrolisis air dengan adanya pemangkin - platinum dan aloi mahal yang lain.
- Campuran gas hidrogen + oksigen (oksigen) sederhana meletup dari percikan sedikitpun, serta-merta melepaskan sejumlah besar tenaga.
Untuk rujukan. Para saintis yang pertama kali memisahkan molekul air menjadi hidrogen dan oksigen memanggil campuran itu sebagai bahan letupan kerana kecenderungannya untuk meletup. Selepas itu, ia menerima nama Brown's gas (dengan nama penemu) dan ditetapkan oleh formula hipotesis NGO.

Dari yang disebutkan sebelumnya, kesimpulan berikut menunjukkan dirinya sendiri: 2 atom hidrogen mudah bergabung dengan 1 atom oksigen, tetapi mereka sangat enggan berpisah. Reaksi pengoksidaan kimia diteruskan dengan pembebasan langsung tenaga termal sesuai dengan formula:
2H2 + O2 → 2H2O + Q (tenaga)
Inilah titik penting yang akan berguna bagi kami dalam analisis penerbangan lebih lanjut: hidrogen masuk ke dalam reaksi secara spontan dari pencucuhan, dan haba dilepaskan secara langsung. Untuk memisahkan molekul air, tenaga perlu dibelanjakan:
2H2O → 2H2 + O2 - Q
Ini adalah formula tindak balas elektrolitik yang mencirikan proses pemisahan air dengan membekalkan elektrik. Cara mempraktikkan ini dan membuat penjana hidrogen dengan tangan anda sendiri, kami akan mempertimbangkan lebih jauh.
Penciptaan prototaip
Untuk membuat anda memahami apa yang anda hadapi, pertama-tama kami sarankan memasang penjana hidrogen termudah dengan kos terendah. Reka bentuk pemasangan buatan rumah ditunjukkan dalam rajah.

Apa yang terdiri daripada elektrolisis primitif:
- reaktor - bekas kaca atau plastik dengan dinding tebal;
- elektrod logam direndam dalam reaktor dengan air dan disambungkan ke sumber kuasa;
- tangki kedua bertindak sebagai penutup air;
- Paip ekzos gas HHO.
Perkara penting. Loji hidrogen elektrolitik hanya beroperasi pada arus terus. Oleh itu, gunakan penyesuai AC, pengecas kereta, atau bateri sebagai sumber kuasa. Alternator tidak akan berfungsi.
Prinsip pengoperasian electrolyzer adalah seperti berikut:
- Dua elektrod yang direndam dalam air dibekalkan dengan voltan, lebih baik dari sumber yang boleh dilaraskan.Untuk memperbaiki tindak balas, sedikit alkali atau asid ditambahkan ke dalam bekas (di rumah - garam biasa).
- Sebagai hasil reaksi elektrolisis, hidrogen akan dilepaskan dari sisi katod yang dihubungkan ke terminal "minus", dan oksigen akan dihasilkan di dekat anoda.
- Mencampurkan, kedua-dua gas melalui tiub memasuki perangkap air yang melakukan 2 fungsi: memisahkan wap air dan mencegah kilat di dalam reaktor.
- Dari tangki kedua, gas letupan NNO disalurkan ke pembakar, di mana ia dibakar untuk membentuk air.
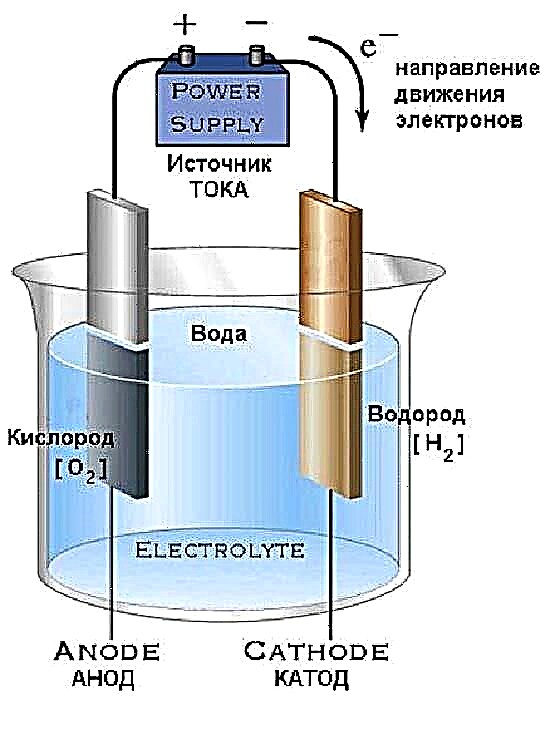
Untuk membuat reka bentuk penjana yang ditunjukkan dalam gambar rajah dengan tangan anda sendiri, anda memerlukan 2 botol kaca dengan leher dan penutup lebar, penitis perubatan dan 2 dozen skru. Satu set lengkap bahan ditunjukkan dalam foto.

Dari alat khas itu, pistol gam diperlukan untuk menutup penutup plastik. Prosedur pembuatannya mudah:
- Putar batang kayu rata dengan skru mengetuk sendiri, meletakkan hujungnya ke arah yang berbeza. Pateri kepala skru bersama-sama dan sambungkan wayar - dapatkan elektrod masa depan.
- Buat lubang di penutup, masukkan bekas potong penitis dan wayar di sana, kemudian tutup pada kedua-dua sisi dengan pistol gam.
- Letakkan elektrod di dalam botol dan skru pada penutupnya.
- Pada penutup kedua, gerudi 2 lubang, masukkan tiub penitis dan skru ke botol berisi air biasa.
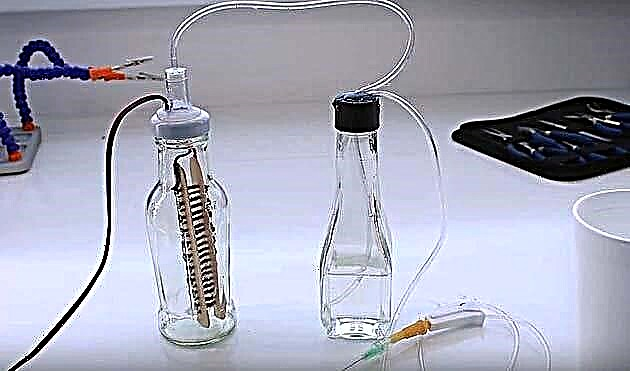
Untuk memulakan penjana hidrogen, tuangkan air masin ke dalam reaktor dan hidupkan sumber kuasa. Permulaan tindak balas ditandai dengan penampilan gelembung gas di kedua-dua bekas. Atur voltan ke nilai optimum dan nyalakan gas Brown yang keluar dari jarum penitis.
Mengenai sel hidrogen Meyer
Sekiranya anda membuat dan menguji reka bentuk yang dijelaskan di atas, maka dengan membakar api di hujung jarum, anda mungkin menyedari bahawa prestasi pemasangannya sangat rendah. Untuk mendapatkan gas yang lebih meletup, anda perlu membuat alat yang lebih serius, yang dipanggil sel Stanley Meyer sebagai penghormatan kepada penemu.
Prinsip operasi sel juga berdasarkan elektrolisis, hanya anod dan katod yang dibuat dalam bentuk tiub yang dimasukkan satu sama lain. Voltan dibekalkan dari generator nadi melalui dua gegelung resonan, yang memungkinkan untuk mengurangkan penggunaan arus dan meningkatkan produktiviti penjana hidrogen. Litar elektronik peranti ditunjukkan dalam gambar:

Nota. Perincian mengenai operasi skema dijelaskan pada sumber http://www.meanders.ru/meiers8.shtml.
Untuk membuat sel Meyer, anda memerlukan:
- sarung silinder yang diperbuat daripada plastik atau kaca plexiglass; tukang sering menggunakan penapis air dengan penutup dan muncung;
- tiub keluli tahan karat dengan diameter 15 dan 20 mm, panjang 97 mm;
- wayar, penebat.

Tiub kalis karat dilekatkan pada dasar dielektrik, wayar yang disambungkan ke penjana dipateri padanya. Sel terdiri dari 9 atau 11 tiub yang diletakkan di dalam kotak plastik atau plexiglass, seperti yang ditunjukkan dalam foto.

Unsur-unsur tersebut dihubungkan sesuai dengan semua skema yang diketahui di Internet, yang meliputi unit elektronik, sel Meyer dan kunci air (nama teknikal adalah gelembung). Atas sebab keselamatan, sistem ini dilengkapi dengan sensor untuk tekanan kritikal dan paras air. Menurut ulasan pengrajin rumah, pemasangan hidrogen seperti itu menggunakan arus pesanan 1 ampere pada voltan 12 V dan mempunyai prestasi yang mencukupi, walaupun jumlah yang tepat tidak tersedia.

Reaktor Plat
Penjana hidrogen berprestasi tinggi yang mampu memastikan operasi pembakar gas diperbuat daripada plat tahan karat berukuran 15 x 10 cm, jumlahnya dari 30 hingga 70 buah. Lubang untuk mengetatkan kancing dibor di dalamnya, dan terminal untuk menyambungkan wayar dipotong di sudut.

Selain logam lembaran gred 316, anda perlu membeli:
- Getah tebal 4 mm tahan alkali;
- plat hujung yang diperbuat daripada plexiglass atau textolite;
- tali leher M10-14;
- periksa injap untuk alat kimpalan gas;
- penapis air di bawah hidrolok;
- menghubungkan paip dari keluli tahan karat bergelombang;
- kalium hidroksida dalam bentuk serbuk.

Plat mesti dipasang ke dalam satu unit, diisolasi antara satu sama lain dengan gasket getah dengan potongan tengah, seperti yang ditunjukkan dalam gambar. Tarik reaktor yang dihasilkan dengan rapat dengan kancing dan sambungkan ke muncung elektrolit. Yang terakhir datang dari bekas berasingan yang dilengkapi dengan penutup dan injap penutup.
Nota. Kami memberitahu bagaimana membuat elektrolisis jenis aliran (kering). Lebih mudah untuk membuat reaktor dengan plat rendaman - anda tidak perlu meletakkan gasket getah, dan unit yang dipasang diturunkan ke dalam bekas tertutup dengan elektrolit.

Pemasangan penjana hidrogen seterusnya dilakukan dengan cara yang sama, tetapi dengan perbezaan:
- Pada selongsong alat dipasang tangki untuk penyediaan elektrolit. Yang terakhir adalah larutan kalium hidroksida 7-15% di dalam air.
- Sebagai ganti air, yang disebut deoxidizer - aseton atau pelarut anorganik - dituangkan ke dalam "bubbler".
- Injap periksa mesti diletakkan di hadapan pembakar, jika tidak, apabila pembakar hidrogen dimatikan dengan lancar, pukulan terbalik akan memecahkan selang dan gelembung.
Adakah menguntungkan hidrogen di rumah?
Jawapan untuk soalan ini bergantung pada ruang lingkup campuran oksigen-hidrogen. Semua gambar dan rajah yang diterbitkan oleh pelbagai sumber dalam talian direka untuk menghasilkan gas HHO untuk tujuan berikut:
- menggunakan hidrogen sebagai bahan bakar untuk kereta;
- bakar hidrogen tanpa api di dalam dandang pemanasan dan dapur;
- memohon kimpalan gas.
Masalah utama yang mengatasi semua kelebihan bahan bakar hidrogen: kos elektrik untuk pembebasan bahan murni melebihi jumlah tenaga yang diterima dari pembakarannya. Apa sahaja yang diklaim oleh penganut teori utopia, kecekapan maksimum elektrolisis mencapai 50%. Ini bermaksud 1 kW haba menghabiskan 2 kW elektrik. Manfaatnya adalah sifar, malah negatif.
 Ingatlah bahawa kita menulis di bahagian pertama. Hidrogen adalah unsur yang sangat aktif dan bertindak balas dengan oksigen sendiri, menghasilkan banyak haba. Cuba memisahkan molekul air yang stabil, kita tidak dapat membawa tenaga secara langsung ke atom. Pembelahan dilakukan dengan menggunakan elektrik, separuh daripadanya dibuang dengan memanaskan elektrod, air, belitan pengubah dan sebagainya.
Ingatlah bahawa kita menulis di bahagian pertama. Hidrogen adalah unsur yang sangat aktif dan bertindak balas dengan oksigen sendiri, menghasilkan banyak haba. Cuba memisahkan molekul air yang stabil, kita tidak dapat membawa tenaga secara langsung ke atom. Pembelahan dilakukan dengan menggunakan elektrik, separuh daripadanya dibuang dengan memanaskan elektrod, air, belitan pengubah dan sebagainya.
Maklumat latar belakang penting. Haba pembakaran hidrogen tentu tiga kali lebih tinggi daripada metana, tetapi - secara jisim. Sekiranya kita membandingkannya mengikut isipadu, maka ketika membakar 1 m³ hidrogen, hanya 3.6 kW tenaga haba yang akan dibebaskan berbanding dengan 11 kW untuk metana. Lagipun, hidrogen adalah unsur kimia paling ringan.
Sekarang pertimbangkan gas peledak yang diperoleh melalui elektrolisis dalam penjana hidrogen buatan sendiri, sebagai bahan bakar untuk keperluan di atas:
- Harga pemasangan akhir, produktiviti dan kecekapan yang rendah menjadikannya tidak menguntungkan untuk membakar hidrogen untuk memanaskan rumah persendirian. Lebih mudah meletakkan dandang elektrik - SEPULUH, induksi atau elektrod - daripada "angin" meter dengan elektrolisis.
- Untuk menggantikan 1 liter petrol untuk sebuah kereta, diperlukan 4.766 liter hidrogen tulen atau 7.150 liter gas peledak, satu pertiga daripadanya adalah oksigen. Pencipta yang paling buruk di Internet belum membuat alat elektrolisis yang mampu memberikan prestasi yang serupa.

- Alat kimpalan gas yang membakar hidrogen lebih padat dan lebih ringan daripada silinder dengan asetilena, propana dan oksigen. Tambahan, suhu api hingga 3000 ° C membolehkan anda bekerja dengan logam apa pun, kos mendapatkan bahan bakar di sini tidak memainkan peranan khas.
Untuk rujukan. Untuk membakar hidrogen dalam dandang, anda perlu merancang semula strukturnya dengan teliti, kerana pembakar hidrogen dapat mencairkan baja apa pun.
Kesimpulannya
Hidrogen dalam komposisi gas NGO yang diperoleh dari penjana hidrogen buatan rumah berguna untuk dua tujuan: eksperimen dan pengelasan gas.Walaupun kita membuang kecekapan rendah elektrolisis dan kos memasangnya bersama dengan elektrik yang habis, tidak cukup produktiviti untuk memanaskan bangunan. Ini juga berlaku untuk enjin petrol kereta penumpang.